"Interactuando más allá del Salòn de Clases"
Docente: Lisbeth C. Madera R.
¿Que es el Numero de Oxidaciòn o Valencia?
Es el número de electrones cedidos, captados o compartidos por un átomo en su combinación química con otro para formar un enlace.
El número de oxidación es positivo si el átomo pierde electrones o los comparte con un átomo que tenga tendencia a captarlos, y será negativo cuando un átomo gane electrones o los comparta con un átomo que tenga tendencia a ceder electrones.
Muchos elementos pueden actuar con varios números de oxidación diferentes, para determinar con qué número de oxidación está actuando un elemento se deben tener en cuantas algunas reglas...
-
El N de oxidación de un átomo en un elemento libre es cero.
-
El N de oxidación de un ion mono-atómico es su propia carga
-
En toda molécula la suma de los números de oxidación es igual a cero.
-
El oxígeno actúa siempre con N de oxidación -2. Existen dos excepciones a esta regla: los peróxidos, en los que el oxígeno actúa con valencia -1; y cuando se combina con el flúor con el que tiene +2.
-
El Hidrógeno combinado con un no metal tiene valencia +1 y con un metal -1.
-
Cuando se unen un metal y un no metal, el metal actúa con N de oxidación positivo y el No metal con negativo.
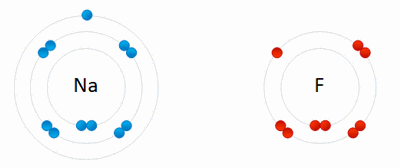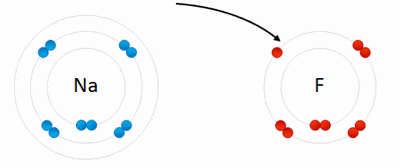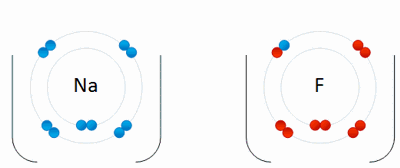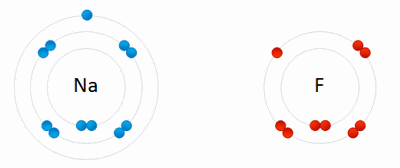
La Regla del Octeto
La regla del octeto, también llamada ley de Lewis, dice que todos los átomos de los elementos del sistema periódico, tienden a completar sus últimos niveles de energía con una cantidad de 8 electrones.
Los gases nobles son los únicos no reactivos, por que ya tienen 8 electrones en su última capa y no admiten más.

ACTIVIDADES
Aprende y Evalúa tus conocimientos sobre los átomos, compuestos químicos, y enlaces. Da clic sobre el botón a tu derecha y juega con
Jclic.Js
¿Que tanto sabes sobre Enlaces Químicos?
Da Clic en el botón a tu derecha y aprende jugando con CELEBRITY
Evalúa tus conocimientos sobre tipos de Enlaces Químicos?
Da Clic en el botón a tu derecha y aprende jugando con CELEBRITY
Evalúa tus conocimientos Descarga y realiza la siguiente actividad
¿Como se unen los átomos?
Los atomos se mantienen unidos a través de "Enlaces Quimicos".
Conocemos como enlaces químicos a la fusión de átomos y moléculas para formar compuestos químicos más grandes y complejos dotados de estabilidad. En este proceso los átomos o moléculas alteran sus propiedades físicas y químicas, constituyendo nuevas sustancias.